Hitung ph NH4OH 0,01 M (kb = 10-6)
Mapel Kimia, Jenjang Sekolah Menengah Atas
Penjelasan:
[OH-] = akar Kb. Mb= akar 10^-6 . 10^-2
= akar 10^-8
= 10^-4
pOH = -log [OH-]
= -log 10^-4
= 4
pH = 14 – pOH
= 14-4 = 10
Pertanyaan Baru di Kimia
Apabila lelehan magnesium klorida dielektrolisis digunakan arus sebanyak 1 Faraday, maka logam magnesium yang dihasilkan sebanyak …. ( Ar Mg =24 ) A
6 gram
B
24 gram
C
2,4 gram
D
12 gram
E
4,8 gram
Kimia, Sekolah Menengah Atas
Jawaban:
D.
Penjelasan:
Elektrolisis: Lelehan MgCl2
katode : Mg^2+ + 2e => Mg
Artinya 1 mol Mg = 2 mol e
Rumus: massa logam ( w ) = e . F
dimana e = Ar / mol e
e = 24 / 2
e = 12
berarti w = 12 . 1 F = 12 g
Kelompokkan struktur senyawa karbon berikut ke dalam senyawa karbon jenuh atau senyawa karbon tidak jenuh.
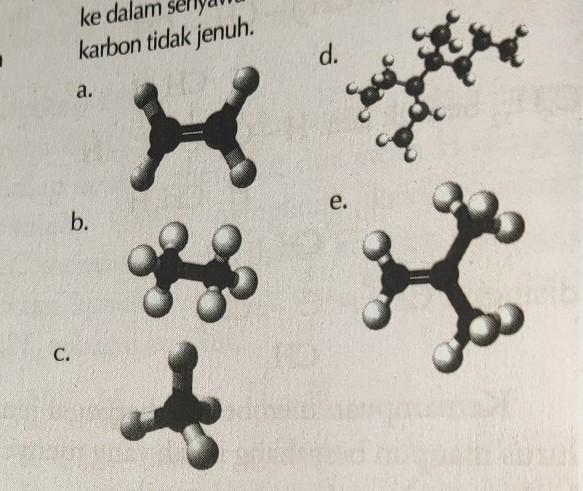
Kimia, Sekolah Menengah Atas
Penjelasan:
penentuan senyawa karbon jenuh dan tak jenuh ditentukan berdasarkan ikatan yang ada di dalam strukturnya. apabila hanya memiliki ikatan tunggal (alkana) maka disebut senyawa karbon jenuh. sedangkan apabila memiliki ikatan rangkap (alkena dan alkuna) maka disebut senyawa karbon tak jenuh.
pada gambar, senyawa a dan e memiliki ikatan rangkap sehingga disebut senyawa karbon tak jenuh
sedangkan b,c, dan d hanya memiliki ikatan tunggal maka disebut senyawa karbon jenuh
Jika kertas lakmus biru dicelupkan ke dalam larutan asam, maka warnanya akan …
Kimia, Sekolah Menengah Pertama
Jawaban:
merah
Penjelasan:
ingat aja kalo merah dicelupkan ke basa maka akan berwarna biru, ketika lakmus biru dicelupkan ke asam maka akan berwarna merah
Mohon pencerahan nya

Kimia, Sekolah Menengah Atas
Jawaban:
Menghitung Mr K2SO4
Mr K2SO4 = ( 2 x Ar K ) + ( 1 x Ar S ) + ( 4 x Ar O )
( 2 x 39 ) + ( 1 x 32 ) + ( 4 x 16 ) = 174
Menghitung mol K
massa K = n x Ar K
3,9 = n x 39
n = 0,1 mol
Menghitung mol K2SO4 dengan perbandingan koefisien:
Koefisien K : K2SO4 = 1 : 1 jadi mol K2SO4 = 0,1 mol
Menghitung massa K2SO4
massa K2SO4 = n x Mr
0,1 mol x 174 = 17,4 gram
Jawaban:
Berikut caranya ya
Semoga membantu 🙂
4, 6 gram H2 so4 dilarutkan dalam air hingga volume 500 ml hitung normalitas
Kimia, Sekolah Menengah Atas
1. hitung mol H2SO4
mol = gr/Mr
= 6/98
= 0,06 mol
2. hitung ekivalen dari H2SO4
(valensi H2SO4 = 2 karena memiliki 2 H+)
eq = mol x val
= 0,06 x 2
= 0,12 eq
3. hitung normalitas
N = eq/V(L)
= 0,12/0,5
= 0,24 N
kalo benar kasih jawaban terbaik, kalo salah komen 🙂
 Desain Grafis Indonesia Kumpulan Berita dan Informasi dari berbagai sumber yang terpercaya
Desain Grafis Indonesia Kumpulan Berita dan Informasi dari berbagai sumber yang terpercaya

