Hitunglah perubahan enthalpy standar ΔH0 pada suhu 250 untuk reaksi berikut : N2H4 (l) + O2 (g) ⇔ NO2 (g) + H2O (l)
Dengan menggunakan enthalpy standar pembentukan (ΔHf0) rekatan dan produk pada suhu 250C
Mapel Kimia, Jenjang Sekolah Menengah Atas
Jawaban:
N₂H₄ + 3O₂ ⇔ 2NO₂ + 2H₂O ( Sudah Setara)
ΔH = ΔHf produk – ΔHf reaktan
ΔH = (2 × ΔHf NO₂ + 2 ΔHf × H₂O) – ( 1 × ΔHf N₂H₄ + 3 × ΔHf O₂ )
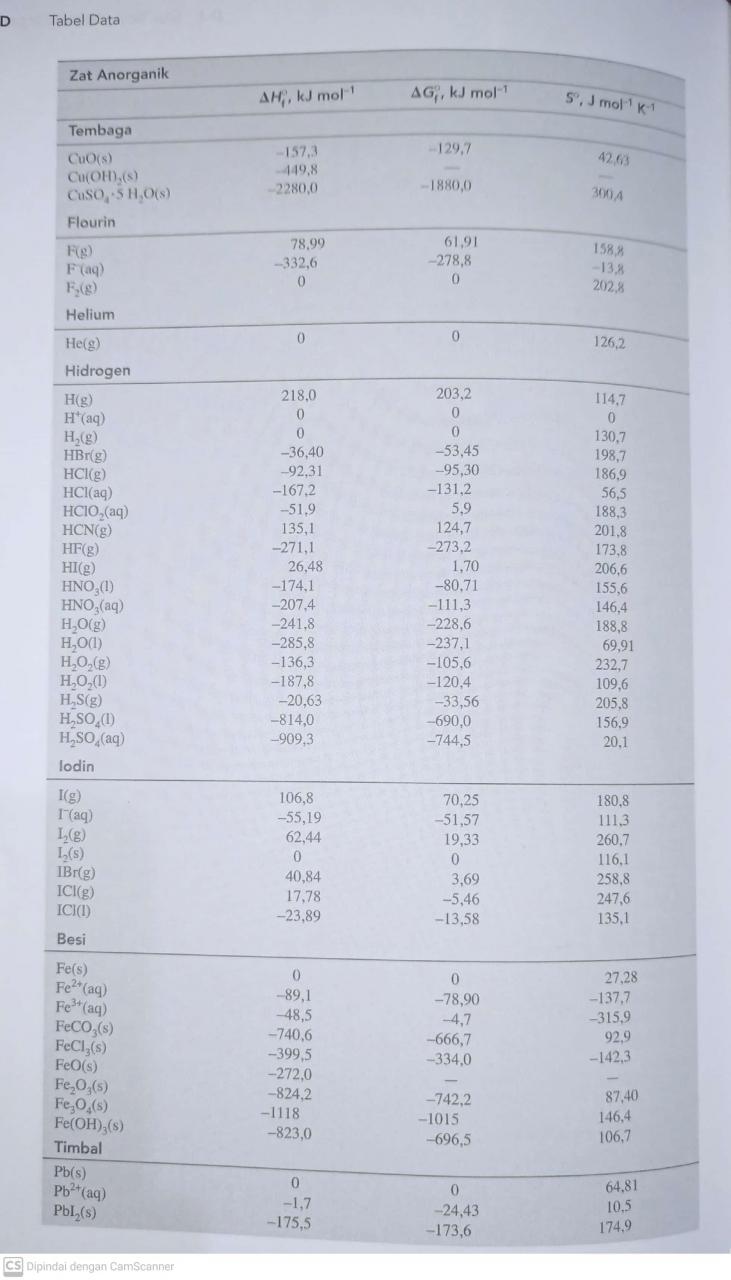
ΔH = ( 2 × 33,18 + 2 × (-285,8)) – ( 1 × 50,63 + 3 × 0)
ΔH = (66,36 + (-571,6)) – 50,63
ΔH = -505,24-50,63
ΔH = -555,87
Penjelasan:
Semoga Bermanfaat makasih, jangan lupa dijadikan jawaban tercerdas ya :v
Pertanyaan Baru di Kimia
Cara pembuatan logam timah hitam
Kimia, Sekolah Menengah Atas
Jawaban:
Secara pengolahan bijih timah menjadi logam timah terdiri dari operasi konsentrasi/mineral dressing, dan ekstraksi yaitu peleburan atau smelting dan pemurnian atau refining.
Timah primer= dihasilkan dari mineralisasi pada intrusi batuan granit (magmatik asam).
Bantu jawab soal kimiaa

Kimia, Sekolah Menengah Atas
Jawaban:
A. 1 dan 2
Penjelasan:
Larutan elektrolit lemah: nyala lampu rendah ataupun tidak menyala, sedangkan msh ada gelembung gas
Larutan elektrolit kuat: nyala lampu terang & banyak gelembung gas
Diketahui pasangan sel volta dengan notasi sel sebagai berikut: Zn/Zn2+//Cu3+/Cu E0= +1,10V
Pb/Pb2+//Cu3+/Cu E0= +0.47V
Sel volta yang tersusun dari pasangan elektrode Zn dan Pb akan mempunyai harga E0sel sebesar ….
Kimia, Sekolah Menengah Atas
Jawaban:
E⁰sel = reduksi – E oksidasi
E⁰sel = 0,47 v – 1,10 v
E⁰sel = -0,63 v
Penjelasan:
Semoga Bermanfaat ya
Dari senyawa-senyawa berikut yang massa molekul relatifnya (mr) paling besar adalah….( ar h = 1, n = 14, c = 12, o = 16, s = 32)
Kimia, Sekolah Menengah Atas
Jawaban:
soalnya kurang lengkap
Penjelasan:
tidak jelas soalnya
Mohon bantuannya buat no 9
#saintek #ujianmandiri #ipa

Kimia, Sekolah Menengah Atas
Jawaban:
B. 365 ml
Penjelasan:
Rumus pengenceran:
V1 . M1 = V2. M2
V1 . 96% = 500 . 70%
V1 = 364,58 ml dibulatkan 365 ml
 Desain Grafis Indonesia Kumpulan Berita dan Informasi dari berbagai sumber yang terpercaya
Desain Grafis Indonesia Kumpulan Berita dan Informasi dari berbagai sumber yang terpercaya

